IP-10 para Diagnóstico e Tratamento da Tuberculose em Crianças

A tuberculose em crianças continua sendo um desafio significativo para a saúde pública, especialmente devido às dificuldades no diagnóstico precoce e à diversidade de apresentações clínicas. Crianças infectadas geralmente desenvolvem formas paucibacilares da doença, o que dificulta a confirmação microbiológica. Além disso, testes diagnósticos convencionais, como o teste tuberculínico (TST) e os ensaios de liberação de interferon-gama (IGRAs), apresentam limitações nessa população. Assim, a busca por biomarcadores mais sensíveis e específicos, como a proteína IP-10, é essencial para aprimorar o diagnóstico e monitorar a resposta ao tratamento antituberculose em pediatria.
Resumo
Objetivo: Determinar a utilidade da proteína 10 induzida por interferon-gama (IP-10) para identificar a tuberculose ativa (TB) e a infecção por tuberculose (TBI) em crianças vacinadas com BCG, estabelecer suas características de desempenho diagnóstico e avaliar as mudanças nos níveis de IP-10 durante a quimioterapia antituberculose.
Métodos: As concentrações de IP-10 e IFN-γ foram medidas em amostras de supernatantes do QuantiFERON-TB Gold (QFT) em crianças com suspeita de TB ou devido ao contato recente com a doença. No total, 225 crianças foram investigadas: 33 com TB ativa, 48 com TBI, 83 contatos de TB, 20 com suspeita de TB mas com diagnósticos alternativos e 41 controles. Em 60 crianças, as respostas de citocinas foram avaliadas em uma visita de acompanhamento após dois meses de tratamento antituberculose.
Resultados: A expressão de IP-10 foi significativamente maior em crianças infectadas (casos de TB ativa e TBI) do que em indivíduos não infectados. O IP-10 mostrou-se eficaz na identificação da infecção por TB no seu ponto de corte ideal (>1084,5 pg/mL), mas não foi capaz de diferenciar entre crianças com TB ativa e TBI. A combinação de IP-10 e IFN-γ aumentou a sensibilidade do QFT. O IP-10, mas não o IFN-γ, diminuiu significativamente durante o tratamento em crianças com TB ativa (p = 0,003).
Conclusão: O IP-10 identifica a infecção por TB e diminui durante o tratamento em crianças. A incorporação do IP-10 em novos testes imunodiagnósticos pode melhorar o diagnóstico da TB e permitir o monitoramento do tratamento.
Palavras-chave: tuberculose, quimiocina CXCL10, Mycobacterium tuberculosis, LTBI, contato com TB
Introdução
A tuberculose infantil, causada pelo Mycobacterium tuberculosis (Mtb.), ainda é um problema urgente de saúde global. Após a pandemia de COVID-19, essa situação se agravou. Devido às interrupções relacionadas à COVID-19 na detecção e tratamento da TB, houve um aumento global na incidência e mortalidade por TB. No entanto, as estimativas epidemiológicas da carga de TB infantil continuam subestimadas por vários motivos:
- A TB ativa em crianças é difícil de diagnosticar devido a apresentações clínicas diversas, dificuldades para obter amostras para avaliação microbiológica e a natureza paucibacilar da doença.
- O diagnóstico da infecção tuberculosa (TBI) carece de um padrão-ouro, e os testes imunológicos utilizados, como o teste cutâneo de tuberculina (TST) e os ensaios de liberação de interferon-gama (IGRAs), apresentam limitações significativas na população pediátrica.
O TST apresenta reatividade cruzada com a vacina BCG e a maioria das micobactérias não tuberculosas (NTM), resultando em baixa especificidade em crianças vacinadas com BCG e infectadas com NTM. Os IGRAs disponíveis comercialmente, como o QuantiFERON-TB Gold In-Tube (QFT) e o T-SPOT.TB, têm sensibilidade comparável e maior especificidade do que o TST para identificar a infecção por Mtb. No entanto, eles não conseguem diferenciar a TB ativa da infecção latente (TBI) e têm desempenho reduzido em crianças pequenas e indivíduos infectados pelo HIV.
Um biomarcador promissor para melhorar o desempenho dos IGRAs é a proteína IP-10, uma quimiocina induzida por interferon-gama (IFN-γ). Estudos sugerem que os ensaios baseados em IP-10 podem ser alternativas aos IGRAs tradicionais, já que a IP-10 é liberada em concentrações 100 vezes maiores que o IFN-γ, facilitando sua detecção. Além disso, a IP-10 tem sido proposta como um biomarcador potencial para monitoramento do tratamento, embora os estudos em populações pediátricas sejam escassos.
O objetivo deste estudo foi avaliar as respostas de IP-10 em crianças com sintomas de TB ativa e em contatos de TB em um país de baixa incidência de TB, onde a vacinação BCG é administrada rotineiramente ao nascimento. Pretendemos examinar o potencial do IP-10 para diferenciar entre diferentes estágios da infecção por Mtb., comparar os resultados do IP-10 com o QFT e o TST, e explorar a influência da idade e do tratamento antituberculose nos níveis de IP-10.
2. Métodos
2.1. População do Estudo
Para este estudo prospectivo, recrutamos crianças menores de 18 anos internadas no Hospital Infantil da Universidade Médica de Varsóvia, Polônia, e no Centro Mazoviano para Tratamento de Doenças Pulmonares e Tuberculose, entre maio de 2012 e setembro de 2015. As crianças elegíveis para participação foram:
- Crianças com suspeita clínica de TB.
- Crianças em contato recente com tuberculose pulmonar (PTB).
Critérios de exclusão: imunossupressão, tratamento anterior para TB e realização do teste de tuberculina (TST) nos últimos 18 meses para minimizar o risco de estímulo adicional.
A aprovação ética foi concedida pelo Comitê de Bioética da Universidade Médica de Varsóvia, e o consentimento informado por escrito foi obtido dos responsáveis legais de cada participante antes do recrutamento.
2.2. Procedimentos Clínicos e Laboratoriais
Dados demográficos, históricos e achados clínicos foram registrados sistematicamente usando um formulário de relatório de caso. Todos os participantes realizaram exames de sangue periférico, incluindo o QuantiFERON-TB Gold (QFT). Crianças com suspeita de TB ou rastreadas por contato passaram por procedimentos diagnósticos padrão, como:
- Teste de tuberculina (TST);
- QuantiFERON-TB Gold (QFT);
- Raio-X de tórax;
- Avaliação histológica e bacteriológica (microscopia, PCR e cultura), quando necessário.
Nem todos os participantes fizeram o TST devido à escassez de derivados de proteína purificada (PPD) durante o período do estudo. Por razões éticas, não realizamos TST, raio-X de tórax ou estudos microbiológicos no grupo controle.
2.2.1. Teste de Tuberculina (TST)
O TST foi realizado com uma injeção intradérmica de 2 unidades de tuberculina (0,1 mL) de RT 23 PPD (Statens Serum Institute, Dinamarca) no braço esquerdo. A induração transversal foi medida após 48 a 72 horas. O TST foi considerado positivo com uma induração ≥ 10 mm.
2.2.2. QuantiFERON-TB GOLD In-Tube
O ensaio QuantiFERON-TB GOLD foi realizado conforme as instruções do fabricante. A concentração de IFN-γ foi determinada usando o ELISA QFT, e os resultados foram definidos utilizando o software Cellestis Version 2.50.1 (Cellestis/Qiagen, Carnegie, Austrália).
2.2.3. Determinação de IP-10
A concentração de IP-10 foi medida nos supernatantes restantes dos tubos QFT utilizando o ensaio Quantikine ELISA Human IP-10 (R&D Systems Europe, Reino Unido), seguindo as instruções do fabricante. As amostras foram medidas em duplicata. O plasma foi diluído 1:10, e amostras com valores fora do limite superior da curva padrão foram diluídas e medidas novamente. O limite inferior de detecção foi calculado em 2,1 pg/mL, e as concentrações de IP-10 foram expressas em pg/mL.
2.3. Classificação dos Participantes
Após a avaliação clínica e diagnóstica, os pacientes foram classificados em cinco categorias:
- TB ativa (ATB): pacientes sintomáticos com confirmação microbiológica ou que preenchiam pelo menos dois dos seguintes critérios:
- Sintomas clínicos sugestivos de TB ativa;
- Achados radiológicos consistentes com TB ativa;
- Histórico de contato com TB pulmonar, em conjunto com resposta positiva ao tratamento.
- Infecção tuberculosa (TBI): crianças assintomáticas com TST e/ou QFT positivo e radiografia de tórax normal.
- Contatos de TB: crianças assintomáticas com histórico de contato com TB, sem critérios para TB ativa ou TBI.
- Não-TB: crianças com suspeita de TB, mas com diagnósticos finais diferentes e resposta positiva ao tratamento específico.
- Controles: crianças assintomáticas, cuidadosamente excluídas de contato com TB e comorbidades inflamatórias, além de resultado negativo no QFT.
2.4. Análise Estatística
Os dados foram analisados usando o software STATISTICA 13.1 (SatSoft, Polônia) e Medcalc 19.1 (MedCalc Software, Bélgica). As figuras foram preparadas no GraphPad Prism versão 8. Os dados são apresentados como medianas e intervalos interquartis (IQRs).
Foram utilizados os seguintes testes estatísticos:
- Teste qui-quadrado ou teste exato de Fisher para variáveis qualitativas;
- Teste de Kruskal-Wallis ou teste de Mann-Whitney para variáveis quantitativas;
- Teste de Wilcoxon para avaliar mudanças nos níveis de IFN-γ e IP-10 durante o tratamento.
A precisão diagnóstica de IP-10 foi avaliada por análise da curva ROC (Receiver Operating Characteristic), e o valor de corte foi selecionado usando o índice de Youden. O nível de significância foi definido como p < 0,05.
3. Resultados
3.1. Características dos Participantes do Estudo
No total, 263 crianças foram consideradas elegíveis para o estudo, mas 38 foram excluídas por diversos motivos:
- Amostras de sangue insuficientes (19 crianças);
- Manuseio inadequado das amostras (2 crianças);
- Dados insuficientes (2 crianças);
- Problemas técnicos (10 crianças);
- Contato com casos diagnosticados com micobactérias não tuberculosas (NTM) em vez de Mycobacterium tuberculosis (5 crianças).
Assim, a análise final incluiu 225 crianças, distribuídas nas seguintes categorias:
- TB ativa (ATB): 33 crianças;
- Infecção tuberculosa (TBI): 48 crianças;
- Contatos de TB: 83 crianças;
- Não-TB: 20 crianças;
- Controles: 41 crianças.
Características demográficas:
- Os pacientes com TB ativa eram mais velhos que os de outros grupos (p < 0,05).
- As crianças do grupo de contato com TB eram mais jovens que as do grupo infectado por Mtb. e o grupo Não-TB (p < 0,01).
- Mais de 96% dos participantes estavam vacinados com BCG.
Diagnóstico confirmado:
- Entre os 33 pacientes com TB ativa, 9 (27,3%) tiveram cultura positiva para Mtb., enquanto 13 (39,4%) foram admitidos com suspeita clínica de TB e 20 (60,6%) devido ao contato recente com TB.
- Todas as crianças com TB ativa tiveram resolução completa dos sintomas após tratamento.
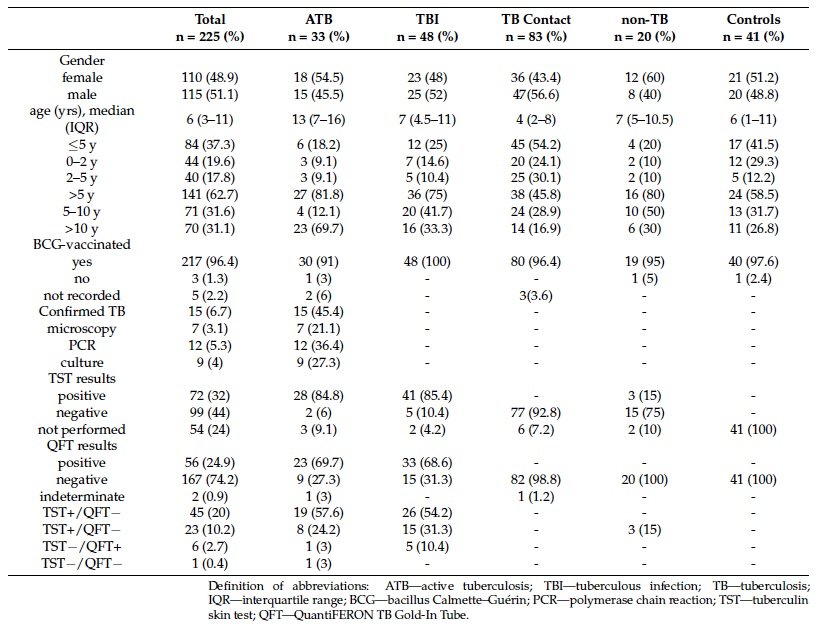
Tabela 1. Características demográficas e clínicas dos participantes do estudo.
3.2. Respostas de IP-10 em Crianças Infectadas e Não Infectadas por Mtb.
As respostas de IP-10 após estimulação com antígeno Mtb. foram significativamente maiores em crianças infectadas (ATB e TBI) em comparação com as não infectadas (p < 0,0001).
Comparação dos níveis de IP-10 entre os grupos:
- Os níveis de IP-10 foram significativamente mais altos no grupo de TB ativa do que no grupo TBI (p = 0,047).
- Não houve diferenças significativas nos níveis de IP-10 entre os grupos Não-TB, Contatos de TB e Controles (p > 0,05).
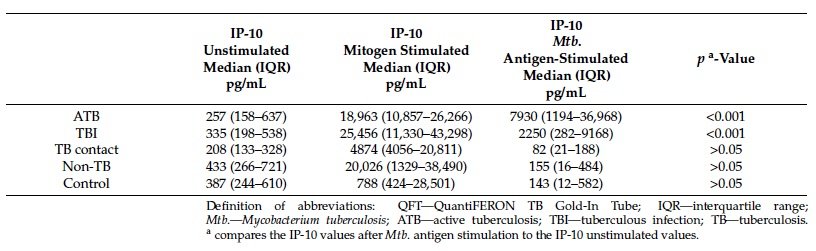
Tabela-2.-Concentracoes-de-IP-10-nos-sobrenadantes-do-QFT
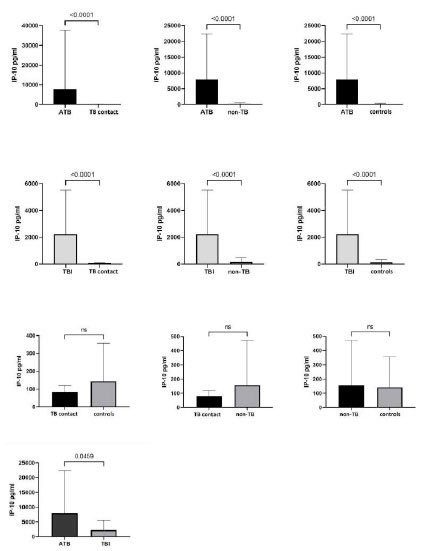
Figura 1. Comparação das respostas de IP-10 estimuladas por antígenos de Mtb. entre os participantes do estudo. ATB — tuberculose ativa; TBI — infecção tuberculosa; TB — tuberculose; ns — não significativo (Mann-Whitney).
3.3. IP-10 Identifica Infecção por Mtb. Independentemente do Motivo da Admissão
Para refletir a prática clínica diária, foi realizada uma análise de subgrupos com base no motivo da admissão hospitalar:
- Suspeita clínica de TB: os níveis de IP-10 foram significativamente mais altos no grupo de TB ativa em comparação com o grupo Não-TB (p < 0,0001).
- Rastreamento de contato: crianças infectadas por Mtb. apresentaram níveis mais altos de IP-10 do que contatos de TB (p < 0,0001).
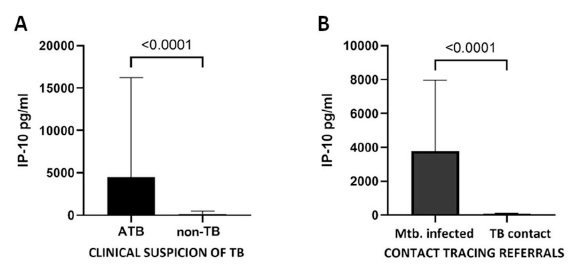
Figura 2. Respostas de IP-10 estimuladas por antígenos de Mtb. em crianças com suspeita clínica de TB (A) e encaminhamentos por rastreamento de contatos (B) (teste de Mann–Whitney).
3.4. Respostas de IP-10 em Relação ao TST, QFT e Resultados Microbiológicos
Dentro do grupo TBI, crianças com resultados concordantes para TST e QFT (TST+QFT+) apresentaram níveis mais altos de IP-10 do que aquelas com resultados discordantes (TST−QFT+ e TST+QFT−).
- Não foram observadas diferenças nos níveis de IP-10 entre crianças com confirmação microbiológica de TB ativa e aquelas sem confirmação.
3.5. Níveis de IP-10 e IFN-γ Não Correlacionam com a Idade
As concentrações de IP-10 e IFN-γ estimuladas pelo antígeno Mtb. variaram entre diferentes faixas etárias, mas a correlação foi fraca para IP-10 (rs = 0,32; p = 0,000001) e insignificante para IFN-γ (rs = 0,16; p = 0,014).
3.6. Nível de IP-10 Diminui Durante o Tratamento Antituberculose
Após dois meses de terapia antituberculose, os níveis de IP-10 foram medidos em 60 crianças:
- 25 com TB ativa;
- 29 com TBI;
- 6 contatos de TB.
Resultados:
- Houve uma redução significativa no nível de IP-10 no grupo com TB ativa (p = 0,0013).
- Nenhuma mudança significativa foi observada no grupo TBI (p = 0,09).
Após a fase inicial do tratamento, os níveis de IP-10 ainda eram significativamente mais altos em crianças com TB ativa do que em contatos de TB (p = 0,0007).
3.7. Desempenho Diagnóstico do IP-10
A análise ROC mostrou que o IP-10 teve excelente desempenho para identificar crianças infectadas por Mtb. (AUC > 0,9), exceto na diferenciação entre TB ativa e TBI.
Ponto de corte ideal: > 1084,5 pg/mL.
- Sensibilidade: 92,68%
- Especificidade: 87,8%
A combinação de IP-10 e QFT aumentou a sensibilidade diagnóstica para 84,5%.
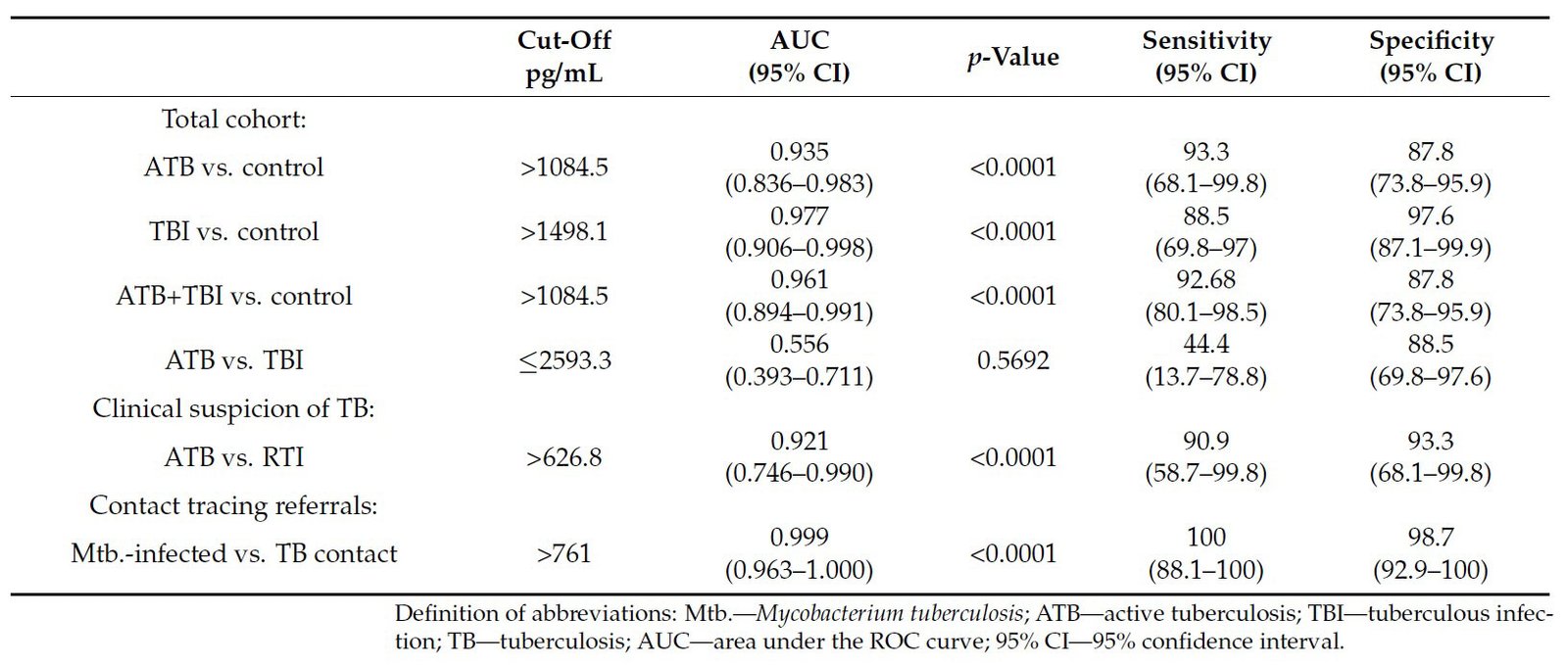
Tabela 3. Análises de características operacionais do receptor (ROC) da IP-10 plasmática para infecção e doença por Mtb.
4. Discussão
O presente estudo indica o potencial do IP-10 para detectar a infecção por Mycobacterium tuberculosis em crianças de um país de baixa incidência de TB, onde a vacinação com BCG é administrada ao nascer. Demonstramos que o nível de IP-10 não está correlacionado com a idade e, pela primeira vez, relatamos uma redução nos níveis de IP-10 durante o tratamento antituberculose em crianças.
Conforme estudos anteriores, mostramos que o IP-10 pode distinguir crianças infectadas por Mtb. daquelas não infectadas. Diferentemente de alguns relatórios, observamos um aumento da expressão de IP-10 apenas em crianças infectadas pelo antígeno Mtb.. Embora diferenças significativas nos níveis de IP-10 entre contatos infectados e não infectados já tenham sido relatadas, poucos estudos investigaram o IP-10 em crianças sintomáticas com suspeita clínica de TB ativa.
No nosso estudo, o IP-10 não foi capaz de diferenciar entre TB ativa (ATB) e infecção tuberculosa latente (TBI) na análise ROC, alinhando-se com a maioria dos relatórios anteriores. Houve, no entanto, uma boa concordância entre o IP-10, o TST e o QFT.
Outro achado importante foi a melhora na sensibilidade diagnóstica quando combinamos os resultados de IP-10 e IFN-γ, especialmente em pacientes com TB ativa, nos quais o desempenho dos IGRAs (ensaios de liberação de IFN-γ) costuma ser subótimo. Estudos anteriores já documentaram os benefícios de uma abordagem combinada de biomarcadores na TB infantil, embora os resultados ainda sejam inconsistentes.
Diferentemente de outros relatórios, não demonstramos uma correlação relevante entre IP-10 e idade. Também não observamos respostas comprometidas de IFN-γ em crianças mais jovens. Além disso, nosso estudo foi o primeiro a relatar uma redução significativa nos níveis de IP-10 durante o tratamento antituberculose em crianças.
Estudos em adultos já haviam sugerido uma diminuição nos níveis de IP-10 após o tratamento bem-sucedido, mas poucos haviam investigado esse efeito em crianças. No nosso estudo, a redução no IP-10 foi detectada apenas em crianças com TB ativa, que apresentavam as maiores concentrações no início do tratamento.
Limitações do Estudo
- O tamanho relativamente pequeno da amostra pode limitar a generalização dos resultados.
- O grupo TBI incluiu crianças com resultados positivos para TST ou QFT, o que pode levar a classificações discordantes e gerar desafios para a interpretação dos resultados.
- A aplicação do critério de QFT negativo para definir os grupos não infectados pode ter introduzido um viés de seleção, dificultando a comparação direta da especificidade do IP-10 com o QFT.
- Crianças com as formas mais graves de TB não foram incluídas, e o desempenho do IP-10 pode diferir nesses casos.
Apesar dessas limitações, acreditamos que nossos critérios rigorosos para diagnóstico de TB ativa minimizaram o risco de classificação incorreta.
5. Conclusão
Nossos dados demonstram que a medição do IP-10 específico para Mtb. tem potencial como biomarcador diagnóstico da TB infantil. Em particular, o IP-10 parece ser um substituto válido para o IFN-γ nos ensaios baseados na plataforma QuantiFERON-TB Gold.
Embora o IP-10 não permita distinguir entre TB ativa e infecção latente, nossos resultados mostram que ele pode ser uma ferramenta eficaz para identificar infecção por Mtb. em crianças com suspeita de TB e para monitorar a resposta ao tratamento.
Essa é a primeira evidência de que o nível de IP-10 diminui significativamente durante a quimioterapia antituberculose em crianças, sugerindo que ele pode ser usado para monitorar o progresso do tratamento.
6. Agradecimentos
Os autores agradecem a Jerzy Ziołkowski, o mentor e idealizador deste estudo, que faleceu em abril de 2014. Agradecemos também à equipe do Departamento de Medicina Laboratorial e Imunologia Clínica da Idade do Desenvolvimento, em especial a Marzena Modzelewska e Elżbieta Widemaier, pelo auxílio na realização dos ensaios de ELISA. O estudo foi financiado pela Universidade Médica de Varsóvia (WUM/1W34/2012/2016).
7. Declarações de Conflito de Interesse
Os autores declaram não haver conflitos de interesse.
8. Referências
A lista de referências inclui uma série de estudos sobre diagnóstico, tratamento e biomarcadores da tuberculose, com destaque para:
- Relatórios da Organização Mundial da Saúde sobre a tuberculose global;
- Estudos sobre o desempenho do QuantiFERON-TB Gold em crianças;
- Pesquisas sobre o potencial do IP-10 como biomarcador para diagnóstico e monitoramento da TB em diferentes populações.
Autores: Agnieszka Strzelak, Anna Komorowska-Piotrowska, Agnieszka Borowa, Maria Krasińska, Wojciech Feleszko, Marek Kulus
Publicação: Diagnostics 2024, 14, 177
DOI: https://doi.org/10.3390/diagnostics14020177
Veja o artigo original completo: Clique aqui!
Evidências apresentadas na World Conference on Lung Health 2025 destacam o potencial clínico e operacional do biomarcador A tuberculose continua
A cidade de Pelotas, localizada no Rio Grande do Sul, encontrou no telemonitoramento uma solução eficaz para enfrentar os desafios
Uma experiência bem-sucedida realizada pelo Distrito Sanitário de Santa Felicidade, em Curitiba (PR), revelou que estratégias simples, criativas e de
Interferon-gamma Inducible Protein 10 como Biomarcador para Tuberculose Ativa e Infecção Latente por Tuberculose em Crianças: Um Estudo Caso-Controle Em